New COVID-19 Treatments 2021
Last updated: 18 March 2025
You can legally access new medicines, even if they are not approved in your country.
Learn howWhat is COVID-19?
Coronavirus disease (COVID-19) is an infectious disease caused by the SARS-CoV-2 virus. It is often called ‘the coronavirus’ or ‘corona’, but the official name of the virus is SARS-CoV-2.1
The SARS-CoV-2 virus is spread through human-to-human transmission. Coughing and sneezing produces small droplets, which can be breathed in by someone else who then becomes infected. The droplets can also be passed on via hand contact, for example if someone touches their nose or face and then shakes hands.1
COVID-19 symptoms
The symptoms are similar to those of the common cold at first. How the disease progresses varies: most people will develop mild to moderate illness, some people do not get sick at all, while others may get seriously ill and sometimes die from the disease.1,2
The most common symptoms of COVID-19 are:1,2
- Cold symptoms (such as a nasal cold, runny nose, sneezing, sore throat)
- Coughing
- Shortness of breath
- Increased temperature or fever
- Sudden loss of taste and/or smell
Less common symptoms of COVID-19 are:1,2
- Tiredness
- Sore throat
- Headache
- Aches and pains
- Diarrhoea
- Various skin abnormalities (such as a rash)
- Eye pain
Treatment of COVID-19
People with mild illness should manage their symptoms at home. It takes on average 5–6 days from infection with the virus for symptoms to show, but it can take up to 14 days. People who are ill in their own home can take paracetamol if they are suffering from pain and fever.1
There are various treatment options for hospitalised patients with COVID-19:1
- Dexamethasone and other corticosteroids, which are used to suppress the immune system.
- Tocilizumab, which is recommended for seriously ill patients.
- Remdesivir, which is an antiviral drug that was approved in 2020.
- Additionally, there are also drugs that have not yet been officially approved, which can already be used in hospitalized patients who have a reduced capacity to produce antibodies against the SARS-CoV-2 virus. These patients receive IV treatment with monoclonal antibodies, which provides them with factory-produced antibodies.
COVID-19 vaccinations
Vaccinations prevent people from becoming seriously ill from a SARS-CoV-2 virus infection. People who are vaccinated are less likely to become infected. If they are infected, their disease symptoms will be less severe, plus they are less contagious.1,3
COVID-19 vaccination side effects
After receiving a significant proportion of people receiving a COVID-19 vaccine have reported side-effects such as fever, headache and tiredness. Side-effects such as muscle pain, joint pain, chills, nausea and vomiting have also been reported after vaccination with COVID-19 vaccines. The side effects also differ depending on which vaccine people received. Women and young people are more likely to have side-effects after vaccination. In very rare cases, more serious side-effects may also occur.1,3
What are new COVID-19 treatments?
There are several approved COVID-19 treatments. Here are some of them:
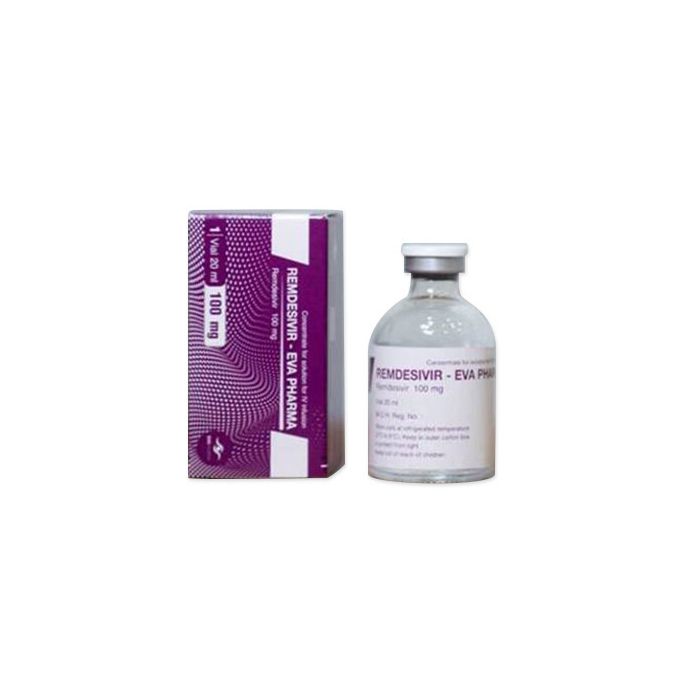
Veklury (remdesivir)
Veklury (remdesivir) is an antiviral medicine used to treat COVID-19. It is used in hospitalized adults and children (aged 12 years and older weighing at least 40 kilograms) requiring supplemental oxygen. It is given via infusion (drip) into a vein. Veklury is the first COVID-19 treatment to receive approval.4,5
Veklury (remdesivir) was approved for the treatment of hospitalized patients with COVID-19 by:
- The European Medicines Agency (EMA) on July 3, 2020.4
- Therapeutic Goods Administration (TGA), Australia on July 10, 2020.6
- Health Canada on July 28, 2020.7
- The Food and Drug Administration (FDA), USA, on October 22, 2020.8
Lagevrio (molnupiravir)
Lagevrio (molnupiravir) is an oral antiviral medicine used to treat mild-to-moderate COVID-19 in adults who are at risk for developing severe illness.9
Lagevrio (molnupiravir) was approved for the treatment of people with mild-to-moderate COVID-19 by:
- The Medicines and Healthcare products Regulatory Agency (MHRA), UK on November 4, 2021.10
This medicine has been given ‘conditional approval’. This means that there is more evidence to come about its efficacy.10
Lagevrio is under review with the U.S. Food and Drug Administration (FDA) and the European Medicines Agency (EMA). The manufacturer Merck is actively working to submit applications to other regulatory agencies around the world.10
Olumiant (baricitinib)
Olumiant (baricitinib) is a medication used for the treatment of rheumatoid arthritis and for the treatment of moderate to severe atopic dermatitis.
On November 19, 2020 the U.S. Food and Drug Administration (FDA) issued an emergency use authorization (EUA) for Olumiant (baricitinib), in combination with Veklury (remdesivir), to treat COVID-19 patients.
Regkirona (regdanvimab)
Regkirona (regdanvimab) is a monoclonal antibody used to treat COVID-19 in adults who do not require supplemental oxygen and who are at increased risk of their disease becoming severe. It is given as a single infusion (drip) into a vein within 7 days of the start of disease symptoms.11,12
Regkirona (regdanvimab) was approved for the treatment of adults with mild-to-moderate COVID-19 by:
- The European Medicines Agency (EMA) on November 12, 2021.11
Ronapreve (casirivimab/imdevimab)
Ronapreve (casirivimab/imdevimab) is a monoclonal antibody used to treat COVID-19 in adults who do not require supplemental oxygen and who are at increased risk of their disease becoming severe. It is given as a single infusion (drip) into a vein within 7 days of the start of disease symptoms.13,14
Ronapreve (casirivimab/imdevimab) was approved for the treatment of adults with mild-to-moderate COVID-19 by:
- The European Medicines Agency (EMA) on November 12, 2021.13
If you are trying to access COVID-19 treatments that are approved outside of your country of residence, we might be able to help you access it with the help of your treating doctor. You can read more about the medicines we can help you access and their price below:
Why access and buy a new treatment for COVID-19 with everyone.org?
everyone.org is registered in The Hague with the Dutch Ministry of Health (registration number 16258 G) as a pharmaceutical wholesale distributor. We have helped patients from over 85 countries to access thousands of medicines including. With a prescription from your treating doctor, you can count on our expert team to safely and legally guide you to access a treatment for COVID-19. If you or someone you know are looking to access a medicine that is not yet approved where they live, we can support you. Contact us for more information.
References:
- RIVM.nl, cited Nov 2021
- Government.nl, cited Nov 2021
- RIVM.nl, cited Nov 2021
- Veklury EMA, Jul 2021
- Veklury product information, EMA, Nov 2021 [PDF]
- TGA, Jul 2021
- Health Canada press release, Jul 2021
- FDA, Oct 2020
- Merck, Nov 2021
- Merck press release, Nov 2021
- Regkirona EMA, Nov 2021
- Regkirona product information, EMA, Nov 2021 [PDF]
- Ronapreve EMA, Nov 2021
- Ronapreve product information, EMA, Nov 2021 [PDF]
Disclaimer: This article is not meant to influence or impact the care provided by your treating physician. Please do not make changes to your treatment without first consulting your healthcare provider. This article is not intended to diagnose or treat illness or to influence treatment options. everyone.org is as diligent as possible in compiling and updating the information on this page. However, everyone.org does not guarantee the correctness and completeness of the information provided on this page.